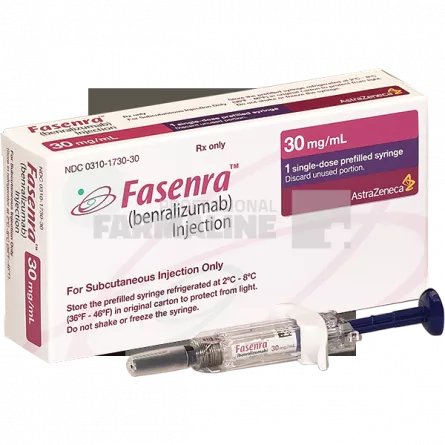
FASENRA 30 mg X 1
ATENTIE!!!
Acest medicament NU se poate comercializa online.
Se eliberează DOAR DIN FARMACIE, STRICT ÎN BAZA REȚETEI MEDICALE. Se poate rezerva online, cu ridicare din farmacie.Pret cu TVA inclus
Descriere
1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI
Fasenra 30 mg soluție injectabilă în seringă preumplută
Fasenra 30 mg soluție injectabilă în stilou injector (pen) preumplut
2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Seringă preumplută
Fiecare seringă preumplută conține benralizumab*30 mg în 1 ml.
Stilou injector (pen) preumplut
Fiecare stilou injector (pen) preumplut conține benralizumab*30 mg în 1 ml.
*Benralizumab este un anticorp monoclonal umanizat produs în celulele ovariene de hamster chinezesc, prin tehnologie ADN recombinant.
Pentru lista tuturor excipienților, vezi pct. 6.1.
3. FORMA FARMACEUTICĂ
Soluție injectabilă în seringă preumplută (injecție)
Soluție injectabilă în stilou injector (pen) preumplut (Fasenra Pen)
Soluție limpede până la opalescentă, incoloră până la galben, care poate să conțină particule transparente, albe sau aproape albe.
4. DATE CLINICE
4.1 Indicații terapeutice
Fasenra este indicat ca terapie adăugată la tratamentul de întreținere la pacienții adulți cu astm bronșic eozinofilic sever, care nu este controlat în mod adecvat prin administrarea inhalatorie a unei doze mari de corticosteroizi plus β-agoniști cu durată lungă de acțiune (vezi pct. 5.1).
4.2 Doze și mod de administrare
Tratamentul cu Fasenra trebuie inițiat de un medic cu experiență în diagnosticarea și tratamentul astmului bronșic sever.
După primirea instrucțiunilor adecvate privind tehnica de injectare subcutanată și a informațiilor despre semnele și simptomele reacțiilor de hipersensibilitate (vezi pct. 4.4), pacienții fără antecedente cunoscute de anafilaxie sau persoanele care îi au în grijă pot administra Fasenra dacă medicul consideră că este potrivit, cu monitorizare medicală dacă este necesar. Auto-administrarea trebuie avută în vedere doar la pacienții care au deja experiență cu tratamentul cu Fasenra.
Doze
Doza recomandată este 30 mg de benralizumab, administrată prin injecție subcutanată, la interval de 4 săptămâni pentru primele 3 doze, apoi la interval de 8 săptămâni. Dacă la data planificată este omisă o injecție, schema terapeutică trebuie reluată cât mai curând posibil, conform schemei de tratament recomandate; nu trebuie administrată o doză dublă.
Fasenra este indicat în tratamentul pe termen lung. Decizia de a continua terapia trebuie stabilită cel puțin anual, în funcție de severitatea afecțiunii, controlul exacerbărilor și numărul eozinofilelor din sânge.
Vârstnici
Nu este necesară ajustarea dozei la vârstnici (vezi pct. 5.2).
Insuficiență renală și hepatică
Nu este necesară ajustarea dozei la pacienții cu insuficiență renală sau hepatică (vezi pct. 5.2).
Copii și adolescenți
Eficacitatea și siguranța Fasenra la copii și adolescenți cu vârsta între 6 și 18 ani nu au fost stabilite.
Nu sunt date disponibile pentru copii cu vârsta între 6 și 11 ani. Datele disponibile în prezent la adolescenți cu vârsta cuprinsă între 12 și 18 ani sunt prezentate la pct. 4.8, 5.1 și 5.2, dar nu se poate face nicio recomandare privind dozele.
Mod de administrare
Fasenra este administrat prin injecție subcutanată.
Fasenra trebuie injectat la nivelul coapsei sau abdomenului. Dacă injecția este administrată de un profesionist în domeniul sănătății sau de o persoană care vă are în grijă, atunci se poate administra și în partea superioară a brațului. Nu trebuie injectat în zone cu tegument sensibil, cu contuzii, eritematos sau cu indurații.
Instrucțiunile detaliate pentru administrare cu seringa preumplută/stiloul injector preumplut (Fasenra Pen) sunt furnizate în „Instrucțiunile de utilizare”
4.3 Contraindicații
Hipersensibilitate la substanța activă sau la oricare dintre excipienții enumerați la pct. 6.1.
4.4 Atenționări și precauții speciale pentru utilizare
Fasenra nu trebuie utilizat în tratamentul acut al exacerbărilor astmului bronșic.
Pacienții trebuie instruiți să solicite asistență medicală în cazul în care astmul bronșic nu este controlat sau dacă se agravează după inițierea tratamentului.
Nu este recomandată întreruperea bruscă a corticoterapiei după iniţierea tratamentului cu Fasenra.
Dacă este necesar, scăderea dozelor de corticosteroizi trebuie să se facă treptat şi sub supravegherea unui medic.
Reacții de hipersensibilitate
Reacții acute sistemice incluzând reacții anafilactice și reacții de hipersensibilitate (de exemplu, urticarie, urticarie papulomatoasă, erupție cutanată tranzitorie) au apărut după administrarea
benralizumab (vezi pct. 4.8). Aceste reacții pot apărea în primele ore de administrare, dar, în unele cazuri, au avut un debut întârziat (adică în câteva zile)
Antecedente de anafilaxie care nu sunt asociate cu administrarea benralizumab pot constitui un factor de risc pentru apariția anafilaxiei după administrarea Fasenra (vexi pct. 4.3.). Conform practicii clinice curente, pacienții trebuie monitorizați o perioadă adecvată de timp după administrarea Fasenra.
În cazul unei reacții de hipersensibilitate, tratamentul cu Fasenra trebuie oprit și trebuie inițiat tratamentul adecvat.
Infecții parazitare (helmintice)
Eozinofilele pot fi implicate în răspunsul imunologic din unele infecții helmintice. Pacienții cu infecții helmintice preexistente au fost excluși de la participarea în studiile clinice. Nu se cunoaște dacă Fasenra poate influența răspunsul pacientului în infecțiile helmintice.
Pacienții cu infecții helmintice preexistente trebuie tratați înaintea inițierii terapiei cu Fasenra. Dacă pacienții dezvoltă o infecție în timpul tratamentului cu Fasenra și nu răspund la tratamentul antihelmintic, tratamentul cu Fasenra trebuie întrerupt până la vindecarea infecției.
4.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Într-un studiu randomizat, cu protocol dublu-orb, cu grupuri paralele, efectuat la 103 pacienți cu vârsta între 12 și 21 de ani cu astm bronșic sever, răspunsul imunității umorale prin anticorpi induși de vaccinarea sezonieră antigripală nu pare să fie afectat de tratamentul cu benralizumab. Nu se așteaptă un efect al benralizumab asupra farmacocineticii medicamentelor administrate concomitent (vezi pct.
5.2).
Enzimele citocromului P450, pompele de eflux și mecanismele de legare de proteinele transport nu sunt implicate în eliminarea benralizumab. Nu există nicio dovadă a exprimării IL-5Rα pe hepatocite.
Depleția eozinofilelor nu determină modificări sistemice cronice ale citokinelor proinflamatorii.
4.6 Fertilitatea, sarcina și alăptarea
Sarcina
Există date limitate (mai puțin de 300 de rezultate obținute din sarcină) privind utilizarea benralizumab la gravide.
Studiile la animale nu indică efecte directe sau indirecte în legătură cu toxicitatea asupra funcției de reproducere (vezi pct. 5.3).
Anticorpii monoclonali, așa cum este benralizumab, traversează placenta în mod liniar, pe măsura avansării sarcinii; astfel, expunerea potențială pentru făt este mai mare în trimestrele al doilea și al treilea de sarcină.
Este de preferat să se evite utilizarea Fasenra în timpul sarcinii. Administrarea la gravide trebuie luată în calcul numai dacă beneficiul aşteptat la mamă este mai mare decât orice risc posibil pentru făt.
Alăptarea
Nu se cunoaște dacă benralizumab sau metaboliții acestuia se excretă în lapte la om sau la animale. Nu poate fi exclus riscul pentru copiii alăptați.
Trebuie luată decizia de întrerupere a alăptării sau de întrerupere/oprire a utilizării Fasenra, având în vedere beneficiul alăptării pentru copil și beneficiul tratamentului pentru femeie.
Fertilitatea
Nu există date privind fertilitatea la om. Studiile la animale nu au arătat efecte adverse ale tratamentului cu benralizumab asupra fertilității (vezi pct. 5.3).
4.7 Efecte asupra capacității de conduce vehicule și de a folosi utilaje
Fasenra nu are nicio influență sau are influență neglijabilă asupra capacității de a conduce vehicule sau de a folosi utilaje.
4.8 Reacții adverse
Rezumatul profilului de siguranță
Cele mai frecvent raportate reacții adverse în timpul tratamentului sunt cefaleea (8%) și faringita (3%).
Au fost raportate reacții anafilactice.
Descrierea reacției adverse selectate
Reacții la nivelul locului de administrare
În studiile clinice controlate cu placebo, reacțiile la locul injectării (de exemplu, durere, eriterm, prurit, papule) au apărut la 2,2% dintre pacienții tratați cu doza recomandată de benralizumab, comparativ cu 1,9% dintre pacienții la care s-a administrat placebo.
Siguranța pe termen lung
Într-un studiu clinic de extensie cu durata de 56 de săptămâni derulat pe pacienții cu astm bronsic din studiile clinice 1, 2 și 3, 842 de pacienți au fost tratați cu Fasenra în doza recomandată și au rămas în studiu. Profilul general al evenimentelor adverse a fost similar cu cel din studiile clinice din astm descrise mai sus.
Copii și adolescenți
Există date limitate la pacienți copii și adolescenți (vezi pct. 5.1). S-a observat că frecvența, tipul și severitatea reacțiilor adverse la adolescenți au fost similare celor raportate pentru adulți.
Raportarea reacțiilor adverse suspectate
Raportarea reacțiilor adverse suspectate după autorizarea medicamentului este importantă. Acest lucru permite monitorizarea continuă a raportului beneficiu/risc al medicamentului. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacție adversă suspectată prin intermediul sistemului național de raportare, astfel cum este menționat în Anexa V.
4.9 Supradozaj
În studiile clinice au fost administrate subcutanat doze de până la 200 mg la pacienți cu astm bronșic
eozinofilic, fără nicio dovadă a apariției toxicităților dependente de doză.
Nu există un tratament specific pentru supradozajul cu benralizumab. Dacă apare supradozajul, pacientul trebuie să primească tratament suportiv, cu monitorizare adecvată, după cum este necesar.
5. PROPRIETĂȚI FARMACOLOGICE
5.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: medicamente pentru tratamentul bolilor obstructive ale căilor respiratorii, alte medicamente pentru tratamentul bolilor obstructive ale căilor respiratorii, codul ATC: R03DX10
Mecanism de acțiune
Benralizumab este un anticorp monoclonal (IgG1, kappa) anti-eozinofilic, umanizat afucozilat. El se leagă cu afinitate și specificitate crescute de subunitatea alfa a receptorului pentru interleukina 5 umană (IL-5Rα). Receptorul pentru IL-5 este exprimat în mod specific pe suprafața eozinofilelor și bazofilelor. Absența fucozei din domeniul Fc al benralizumab are ca rezultat creșterea afinității pentru receptorii FcɣRIII de pe celulele imune efectoare, așa cum sunt celulele natural killer (NK). Aceasta determină apoptoza eozinofilelor și bazofilelor prin procesul de accentuare a citotoxicității mediate celular dependente de anticorpi (ADCC), reducând inflamația eozinofilică.
Efecte farmacodinamice
Efectul asupra eozinofilelor sanguine
Tratamentul cu benralizumab determină depleția aproape completă a eozinofilelor sanguine în primele 24 de ore după administrarea primei doze, efect menținut pe toată perioada de tratament. Depleția eozinofilelor sanguine este însoțită de o reducere a proteinelor granulare eozinofilice - neurotoxina derivată din eozinofile (EDN) și proteina cationică eozinofilică (ECP) și de reducerea numărului bazofilelor sanguine.
Efectul asupra eozinofilelor din mucoasa bronșică
La pacienții cu astm bronșic și număr crescut de eozinofile în spută (cel puțin 2,5%), efectul benralizumab asupra eozinofilelor din mucoasa bronșică a fost evaluat într-un studiu clinic de fază 1, randomizat, dublu-orb, controlat cu placebo, cu durata de 12 săptămâni, benralizumab fiind administrat subcutanat SC în doze de 100 mg sau 200 mg. În acest studiu, în grupul de tratament cu
benralizumab a fost observată o reducere mediană de 96% față de momentul inițial a numărului eozinofilelor din mucoasa bronșică, comparativ cu o reducere de 47% în grupul la care s-a administrat placebo (p=0,039).
Eficacitate clinică
Eficacitatea Fasenra a fost evaluată în 3 studii clinice randomizate, cu protocol dublu-orb, controlate cu placebo, cu grupuri paralele, cu durate între 28 și 56 de săptămâni, efectuate la pacienți cu vârsta între 12 și 75 de ani.
În aceste studii, Fasenra a fost administrat în doză de 30 mg la interval de 4 săptămâni pentru primele 3 doze și în continuare la interval de 4 sau 8 săptămâni ca terapie adăugată la tratamentul de fond și a fost evaluat în comparație cu placebo.
Cele două studii privind exacerbările, SIROCCO (Studiul 1) și CALIMA (Studiul 2), au inclus în total 2510 pacienți cu astm bronșic sever necontrolat, 64% femei, cu vârsta medie de 49 de ani. Pacienții au avut în antecedente cel puțin 2 exacerbări ale astmului bronșic care a necesitat tratament cu corticosteroizi cu administrare orală sau sistemică (medie de 3) în ultimele 12 luni, scor ACQ-6 de 1,5 sau mai mult la screening și reducerea funcției pulmonare la momentul inițial (modificare medie anticipată a volumului expirator forțat într-o secundă [VEMS] pre-bronhodilatator de 57,5%), în pofida tratamentului regulat cu corticosteroid cu administrare inhalatorie (CSI) în doză mare (Studiul 1) sau cu doză de CSI medie sau mare (Studiul 2) plus un β-agonist cu durată lungă de acțiune (BADLA); cel puțin un tratament de control a fost administrat la 51% și respectiv 41% dintre acești pacienți.
În studiul privind reducerea dozei de corticosteroid cu administrare orală (CSO), ZONDA (Studiul 3), au fost înrolați în total 220 de pacienți cu astm bronșic (61% femei; vârsta medie de 51 de ani), tratați cu CSO zilnic (8 până la 40 mg/zi; media de 10 mg) în plus față de administrarea regulată de CSI în doză mare și un β-agonist cu durată lungă de acțiune (BADLA), cu cel puțin un tratament de control în 53% din cazuri. Studiul a inclus o perioadă de inducție de 8 săptămâni, în care doza CSO a fost stabilită treptat până la doza minimă eficace, fără pierderea controlului astmului bronșic. Pacienții au avut numărul de eozinofile sanguine ≥150 celule/μl și cel puțin o exacerbare în ultimele 12 luni.
Având în vedere că în Studiile 1, 2 și 3 au fost evaluate 2 scheme terapeutice, schema terapeutică recomandată de administrare pentru Fasenra este la interval de 4 săptămâni pentru primele 3 doze și, în continuare, la interval de 8 săptămâni (vezi pct. 4.2), pe baza faptului că nu a fost observat niciun beneficiu dacă administrarea a fost mai frecventă. Rezultatele au fost rezumate mai jos pentru schema terapeutică recomandată.
Studii cu privire la exacerbări
Criteriul principal de evaluare a fost rata anuală a exacerbărilor astmului bronșic semnificative clinic la pacienți cu număr inițial de eozinofile sanguine ≥300 celule/μl, tratați cu doză mare de CSI și un β-agonist cu durată lungă de acțiune. Exacerbarea semnificativă clinic a astmului bronșic a fost definită prin agravarea astmului bronșic, care a necesitat administrarea orală/sistemică de
corticosteroizi timp decel puțin 3 zile și/sau prezentare la camera de gardă, cu necesitate a utilizării orale/sistemice de corticosteroizi și/sau spitalizare. Pentru pacienții aflați în tratament de menținere cu corticosteroizi cu administrare orală, exacerbările au fost definite ca necesitatea unei creșteri temporare a dozei de corticosteroizi cu administrare orală/sistemică pe o perioadă de cel puțin 3 zile sau necesitatea administrării injectabile a unei doze unice de corticosteroizi, de tip depozit.
În ambele studii, în rândul pacienților cu număr al eozinofilelor sanguine ≥300 celule/μl, pacienții tratați cu Fasenra au prezentat reducerea semnificativă a ratei anuale a exacerbărilor, comparativ cu placebo. În plus, din punct de vedere al modificării VEMS mediu, față de momentul inițial, beneficiul a fost observat începând după 4 săptămâni de terapie, acesta menținându-se până la finalul tratamentului.
5.2 Proprietăți farmacocinetice
Farmacocinetica benralizumab a fost direct proporțională cu doza la pacienții cu astm bronșic după administrarea subcutanată a dozelor din intervalul 2 - 200 mg.
Absorbție
După administrarea subcutanată la pacienții cu astm bronșic, timpul de înjumătățire plasmatică a fost de 3,5 zile. Pe baza analizelor de farmacocinetică populațională, biodisponibilitatea absolută estimată a fost de aproximativ 59% și nu a fost observată nicio diferență relevantă clinic privind biodisponibilitatea relativă în cazul administrării la nivelul abdomenului, coapsei sau brațului.
Distribuție
Pe baza analizei de farmacocinetică populațională, volumul de distribuție central și periferic al benralizumab a fost de 3,1 l și, respectiv de 2,5 l, pentru o persoană cu greutatea de 70 kg.
Metabolizare
Benralizumab este un anticorp monoclonal IgG1, care este degradat de enzimele proteolitice cu o largă distribuție în organism, nu numai în țesutul hepatic.
Eliminare
O analiză de farmacocinetică populațională arată că benralizumab prezintă o farmacocinetică liniară, fără dovezi privind o cale de clearance mediată de receptorul țintă. Clearance-ul (Cl) sistemic estimat pentru benralizumab a fost de 0,29 l/zi. După administrarea subcutanată, timpul de înjumătățire plasmatică prin eliminare a fost de aproximativ 15,5 zile.
Grupe speciale de pacienți
Vârstnici (vârsta ≥65 ani)
Pe baza unei analize de farmacocinetică populațională, vârsta nu a influențat clearance-ul benralizumab. Cu toate acestea, nu există date disponibile la pacienții cu vârsta peste 75 de ani.
Copii și adolescenți
Pe baza unei analize de farmacocinetică populațională, farmacocinetica benralizumab la adolescenți cu vârsta de la 12 la17 ani a fost similară celei observate la adulți. Benralizumab nu a fost studiat la copii (vârsta 5 – 11 ani) (vezi pct. 4.2).
Sex, rasă
O analiză de farmacocinetică populațională a arătat că nu există niciun efect semnificativ al sexului și rasei asupra clearance-ului benralizumab.
Insuficiență renală
Nu au fost realizate studii clinice specifice pentru a investiga efectul insuficienței renale asupra benralizumab. Pe baza unei analize de farmacocinetică populațională, clearance-ul benralizumab a fost comparabil la persoane cu valori ale clearance-ului creatininei între 30 și 80 ml/min și pacienți cu funcție renală normală. Sunt disponibile date limitate la pacienți cu clearance-ul creatininei cu valori sub 30 ml/min; totuși, benralizumab nu este excretat renal.
Insuficiență hepatică
Nu au fost realizate studii clinice specifice pentru a investiga efectul insuficienței hepatice asupra benralizumab. Anticorpii monoclonali IgG nu sunt excretați în mod principal la nivel hepatic; nu se anticipează ca modificarea funcției hepatice să influențeze clearance-ul benralizumab. Pe baza analizei de farmacocinetică populațională, nivelul inițial al biomarkerilor funcției hepatice (ALT, AST și bilirubină) nu au avut niciun efect clinic relevant asupra clearance-ului benralizumab.
Interacțiuni medicamentoase
Nu se anticipează un efect al benralizumab asupra farmacocineticii medicamentelor administrate concomitent. Pe baza analizei de farmacocinetică populațională, medicamentele administrate concomitent în mod frecvent (montelukast, paracetamol, inhibitori ai pompei de protoni, antibiotice macrolide și teofilină/aminofilină) nu au avut niciun efect asupra clearance-ului benralizumab la pacienții cu astm bronșic.
5.3 Date preclinice de siguranță
Având în vedere că benralizumab este un anticorp monoclonal, nu au fost realizate studii de genotoxicitate sau carcinogenitate.
Studii toxicologice și/sau farmacologice la animale
Datele non-clinice nu au evidențiat niciun risc special pentru om pe baza studiilor convenționale farmacologice privind evaluarea siguranței sau toxicitatea după doze repetate la maimuțe.
Administrarea intravenoasă și subcutanată la maimuțele cynomolgus s-a asociat cu scăderea numărului eozinofilelor în sângele periferic și în măduva osoasă, fără rezultate toxicologice.
Sarcina
Într-un studiu privind dezvoltarea prenatală și postnatală efectuat la maimuțele cynomolgus gestante, nu au fost observate efecte materne, embrio-fetale sau postnatale asociate cu benralizumab.
Fertilitatea
Nu s-au efectuat studii specifice la animale. Nu a fost observată afectarea asociată cu benralizumab a parametrilor funcției de reproducere la maimuțele cynomolgus masculi și femele. Examinarea parametrilor de fertilitate surogat (inclusiv greutatea organelor și histopatologia țesuturilor organelor de reproducere) la animalele tratate cu benralizumab nu a sugerat nicio afectare a fertilității. Cu toate acestea, în timpul gestației, la puii de maimuță s-a observat o reducere a numărului eozinofilelor.
6. PROPRIETĂȚI FARMACEUTICE
6.1 Lista excipienților
Histidină
Clorhidrat de histidină monohidrat
Dihidrat de trehaloză
Polisorbat 20
Apă pentru preparate injectabile
6.2 Incompatibilități
În absența studiilor de compatibilitate, acest medicament nu trebuie amestecat cu alte medicamente.
6.3 Perioada de valabilitate
3 ani
6.4 Precauții speciale pentru păstrare
A se păstra la frigider (2°C - 8°C). Fasenra poate fi păstrat la temperatura camerei până la 25°C maximum 14 zile. După ce este scos din frigider, Fasenra trebuie utilizat în termen de 14 zile sau aruncat. A se păstra seringa preumplută/stiloul injector preumplut (Fasenra Pen) în ambalajul original pentru a fi protejată/protejat de lumină.
A nu se congela. A nu se agita. A nu se expune la căldură.
6.5 Natura și conținutul ambalajului
Seringa preumplută
Un ml de soluție injectabilă în seringă preumplută de unică folosință, din sticlă de tip I, cu ac încorporat din oțel inoxidabil de mărimea 29G ½ - inch (12,7 mm), capac rigid al acului și piston cu opritor învelit în FluroTec în poziția de siguranță.
Cutie cu 1 seringă preumplută de unică folosință.
Stiloul injector (pen) preumplut
Un ml de soluție injectabilă în stiloul injector (pen) preumplut de unică folosință, steril, din sticlă de tip I, cu ac încorporat din oțel inoxidabil de mărimea 29G ½ - inch (12,7 mm), capac rigid al acului și piston cu opritor învelit în FluroTec într-un stilou injector (pen) preumplut.
Cutie cu 1 stilou injector (pen) preumplut de unică folosință (Fasenra Pen).
6.6 Precauții speciale pentru eliminarea reziduurilor și alte instrucțiuni de manipulare
Fasenra soluție injectabilă este ambalat într-o seringă preumplută de unică folosință, sterilă sau stilou injector (pen) steril pentru uz individual. A nu se agita. A nu se congela.
Înainte de administrare, lăsați cutia cu Fasenra să se încălzească la temperatura camerei. Acest lucru durează în general 30 de minute.
Înainte de administrare, inspectați vizual Fasenra pentru observarea particulelor solide și a modificărilor de culoare. Fasenra este o soluție limpede până la opalescentă, incoloră până la galben, care poate să conțină particule transparente albe sau aproape albe. Nu utilizați Fasenra dacă soluția este tulbure, are modificări de culoare sau atunci când conține particule mari sau corpi străini.
Informații suplimentare și instrucțiuni pentru pregătirea și administrarea Fasenra utilizând seringa preumplută sau stiloul injector preumplut (Fasenra Pen) sunt furnizate în prospect și „Instrucțiuni de utilizare”.
Orice medicament neutilizat sau material rezidual trebuie eliminat în conformitate cu reglementările locale.
7. DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
AstraZeneca AB
SE-151 85 Södertälje
Suedia
8. NUMĂRUL(ELE) AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
EU/1/17/1252/001 1 seringă preumplută
EU/1/17/1252/002 1 stilou injector (pen) preumplut
Review-uri
Pareri FASENRA 30 mg X 1
Fii primul care sparge gheata!
Spune-ne parerea ta despre acest produs si porneste discutia.
Detii sau ai utilizat produsul?
Clientii pfarma.ro nu au adaugat inca opinii pentru acest produs. Fii primul care adauga o parere, folosind formularul de mai jos.
Alerta de pret
Produse similare
Ser fiziologic 90 mg/10 ml 5 fiole
Acesta este un medicament OTC si se poate elibera fara prescriptie medicala. Conform legislatiei in vigoare, pentru a-l putea comanda online...
ALOXI 500mcg x 1 CAPS. MOI 500mcg HELSINN BIREX PHARMA CSC - ANGELINI
Ce este Aloxi? Aloxi este un medicament care conține substanța activă palonosetron. Este disponibil sub formă de soluție injectabilă (250 micrograme în 5 ml de soluție) și sub formă de...
BETABIOPTAL 1,3 mg/g+2,5 mg/g X 1 GEL OFT. 1,3mg/g+2,5mg/g THEA FARMA S.P.A.
Indicații BETABIOPTAL gel este indicat în infecţii oftalmice nepurulente cu bacterii sensibile la cloramfenicol când este utilă asocierea acţiunii antiinflamatoare a betametazonei, în...
CIMZIA x 2 SOL. INJ. IN SERINGA PREUMPLUT 200 mg UCB PHARMA SA
Indicații Artrită reumatoidă Cimzia, în asociere cu metotrexatul (MTX), este indicat pentru: tratamentul poliartritei reumatoide active, moderată până la severă, la pacienţii adulţi,...
LODOZ 2,5mg/6,25mg x 30 COMPR. FILM. 2,5mg/6,25mg MERCK KGAA
Indicații Hipertensiune arterială esenţială uşoară sau moderată. Dozaj Doze Doza iniţială obişnuită este de un comprimat filmat de Lodoz 2,5 mg/6,25 mg o dată pe...
ZYPADHERA 300mg x 1 PULB. + SOLV. PT. SUSP. INJ. C 300mg ELI LILLY NEDERLAND
Zypadhera este un medicament sub forma de pulbere si solvent din care se obtine o suspensie injectabila cu eliberare prelungita. Acesta contine substanta activa olanzapina. „Eliberare...
ZYPREXA 10 mg x 28 COMPR. FILM. 10mg ELI LILLY NEDERLAND
1. CE ESTE ZYPREXA ŞI PENTRU CE SE UTILIZEAZĂ ZYPREXA aparţine grupului de medicamente denumit antipsihotice. ZYPREXA se foloseşte pentru tratamentul unei boli cu simptome cum ar fi:...
HIDRASEC 100 mg X 20 CAPS. 100mg BIOPROJET PHARMA - ABBOTT MYLAN
Ce este Hidrasec si pentru ce se utilizeaza Indicatii Hidrasec 100 mg capsule este indicat in tratamentul diareei acute la adulti. Daca se initiaza tratamentul etiologic al...
QUETIAPINA ZENTIVA 300 mg X 60 COMPR. ELIB. PREL. 300mg ZENTIVA K.S.
Indicații Quetiapină Zentiva comprimate cu eliberare prelungită este indicată pentru: Tratamentul schizofreniei. Tratamentul tulburării bipolare: - episoade maniacale moderate până...
QUETIAPINA ZENTIVA 50 mg X 60 COMPR. ELIB. PREL. 50mg ZENTIVA K.S.
Indicații Quetiapină Zentiva comprimate cu eliberare prelungită este indicată pentru: Tratamentul schizofreniei. Tratamentul tulburării bipolare: - episoade maniacale moderate până...
MILURIT 100 mg x 60 COMPR. 100mg EGIS PHARMACEUTICALS
Ce găsiţi în acest prospect: 1. Ce este Milurit şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să utilizaţi Milurit 3. Cum să utilizaţi Milurit 4. Reacţii adverse posibile...
OLSSA 40 mg/10 mg X 28 COMPR. FILM. 40mg/10mg HCS BVBA - KRKA
Ce găsiți în acest prospect: 1. Ce este Olssa și pentru ce se utilizează 2. Ce trebuie să știți înainte să luați Olssa 3. Cum să luați Olssa 4. Reacții adverse posibile...
TANDESAR 32 mg X 28 COMPR. 32mg TERAPIA S.A.
În acest prospect găsiţi: 1. Ce este Tandesar şi pentru ce se utilizează 2. Înainte să luaţi Tandesar 3. Cum să luaţi Tandesar 4. Reacţii adverse posibile 5. Cum se păstrează Tandesar...
OVESTIN 0,5 mg X 15 OVULE 0,5 mg ASPEN PHARMA TRADING
1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Ovestin 0,5 mg ovule 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare ovul conţine estriol 0,5 mg Pentru lista tuturor excipienţilor, vezi...
DEPAKINE CHRONO 300 mg X 100 COMPR. ELIB. PREL. 300mg SANOFI ROMANIA SRL
Ce găsiţi în acest prospect: 1. Ce este Depakine Chrono şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să luaţi Depakine Chrono 3. Cum să luaţi Depakine Chrono 4. Reacţii...
ZINNAT 500 mg X 10 COMPR. FILM. 500mg GLAXOSMITHKLINE (IRE
1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI Zinnat 500 mg, comprimate filmate 2. COMPOZIŢIA CALITATIVĂ ŞI CANTITATIVĂ Fiecare comprimat filmat conţine cefuroximă 500 mg sub formă de...
VENTOLIN 100 INHALER CFC-FREE X 1 SUSP. INHAL. PRESURIZATA 100µg/doza GLAXOSMITHKLINE (IRE
Ce găsiţi în acest prospect: 1. Ce este Ventolin 100 Inhaler CFC-Free şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să utilizaţi Ventolin 100 Inhaler CFC-Free...
SERETIDE DISKUS 50 micrograme/100 micrograme X 1 PULB. INHAL.
Ce găsiţi în acest prospect: 1. Ce este Seretide Diskus şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să utilizaţi Seretide Diskus 3. Cum să utilizaţi Seretide Diskus 4....
THYROZOL 20mg X 50 COMPR. FILM.
Ce găsiţi în acest prospect: 1. Ce este Thyrozol şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să utilizaţi Thyrozol 3. Cum să utilizaţi Thyrozol 4. Reacţii adverse...
DAVIA 10 mg x 30 COMPR. FIL 10mg TERAPIA
Ce găsiţi ȋn acest prospect: 1. Ce este Davia şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să utilizaţi Davia 3. Cum să utilizaţi Davia 4. Reacţii adverse posibile 5....
RASAGILINA RATIOPHARM 1 mg X 30 COMPR. 1mg TEVA
Ce găsiți în acest prospect 1. Ce este Rasagilină ratiopharm și pentru ce se utilizează 2. Ce trebuie să știți înainte să luați Rasagilină ratiopharm 3. Cum să luați Rasagilină ratiopharm...
FORXIGA 10 mg X 90 COMPR. FILM. 10mg ASTRAZENECA
Ce găsiți în acest prospect 1. Ce este Forxiga și pentru ce se utilizează 2. Ce trebuie să știți înainte să luați Forxiga 3. Cum să luați Forxiga 4. Reacții adverse posibile 5. Cum...
RILUTEK 50 mg X 56 COMPR. FILM. 50mg SANOFI
Ce găsiţi în acest prospect: 1. Ce este RILUTEK şi pentru ce se utilizează 2. Ce trebuie să ştiţi înainte să luaţi RILUTEK 3. Cum să luaţi RILUTEK 4. Reacţii adverse posibile 5. Cum...

.jpg.webp)



![[ALOXI 500mcg x 1 CAPS. MOI 500mcg HELSINN BIREX PHARMA CSC - ANGELINI][Medicamente cu reteta] ALOXI 500mcg x 1 CAPS. MOI 500mcg HELSINN BIREX PHARMA CSC - ANGELINI](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//aloxi-500mcg-x-1-caps.-moi-500mcg-helsinn-birex-ph_173023_1_1520254005.jpg.webp)

![[BETABIOPTAL 1,3 mg/g+2,5 mg/g X 1 GEL OFT. 1,3mg/g+2,5mg/g THEA FARMA S.P.A.][Medicamente cu reteta] BETABIOPTAL 1,3 mg/g+2,5 mg/g X 1 GEL OFT. 1,3mg/g+2,5mg/g THEA FARMA S.P.A.](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//betabioptal-13-mgg25-mgg-x-1-gel-oft-13mgg_173152_1_1521115882.JPG)

![[CIMZIA x 2 SOL. INJ. IN SERINGA PREUMPLUT 200 mg UCB PHARMA SA][Medicamente cu reteta] CIMZIA x 2 SOL. INJ. IN SERINGA PREUMPLUT 200 mg UCB PHARMA SA](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//cimzia-x-2-sol-inj-in-seringa-preumplut-200-mg-u_173273_1_1521707956.jpg.webp)

![[OSETRON 4 mg SOLUTIE INJECTABILA x 5 SOL. INJ. 2mg/ml DR. REDDY'S LABORATO][Medicamente cu reteta] OSETRON 4 mg SOLUTIE INJECTABILA x 5 SOL. INJ. 2mg/ml DR. REDDY'S LABORATO](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//osetron-4-mg-solutie-injectabila-x-5-sol-inj-2mg_173522_2_1523360736.jpg.webp)

![[LODOZ 2,5mg/6,25mg x 30 COMPR. FILM. 2,5mg/6,25mg MERCK KGAA][Medicamente cu reteta] LODOZ 2,5mg/6,25mg x 30 COMPR. FILM. 2,5mg/6,25mg MERCK KGAA](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//lodoz-25mg625mg-x-30-compr-film-25mg625mg-_173957_1_1524817556.jpg.webp)

![[ZYPADHERA 300mg x 1 PULB. + SOLV. PT. SUSP. INJ. C 300mg ELI LILLY NEDERLAND][Medicamente cu reteta] ZYPADHERA 300mg x 1 PULB. + SOLV. PT. SUSP. INJ. C 300mg ELI LILLY NEDERLAND](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//zypadhera-300mg-x-1-pulb-solv-pt-susp-inj-c_174204_1_1525204843.jpg.webp)

![[ZYPREXA 10 mg x 28 COMPR. FILM. 10mg ELI LILLY NEDERLAND][Medicamente cu reteta] ZYPREXA 10 mg x 28 COMPR. FILM. 10mg ELI LILLY NEDERLAND](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//zyprexa-10-mg-x-28-compr-film-10mg-eli-lilly-ned_174206_1_1525205154.jpg.webp)

![[HIDRASEC 100 mg X 20 CAPS. 100mg BIOPROJET PHARMA - ABBOTT MYLAN ][Medicamente cu reteta] HIDRASEC 100 mg X 20 CAPS. 100mg BIOPROJET PHARMA - ABBOTT MYLAN](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//hidrasec-100-mg-x-20-caps-100mg-bioprojet-pharma-_174281_1_1526449340.jpg.webp)

![[QUETIAPINA ZENTIVA 300 mg X 60 COMPR. ELIB. PREL. 300mg ZENTIVA K.S. ][Medicamente cu reteta] QUETIAPINA ZENTIVA 300 mg X 60 COMPR. ELIB. PREL. 300mg ZENTIVA K.S.](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//quetiapina-zentiva-300-mg-x-60-compr-elib-prel-_174333_1_1526889077.jpg.webp)

![[QUETIAPINA ZENTIVA 50 mg X 60 COMPR. ELIB. PREL. 50mg ZENTIVA K.S. ][Medicamente cu reteta] QUETIAPINA ZENTIVA 50 mg X 60 COMPR. ELIB. PREL. 50mg ZENTIVA K.S.](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//quetiapina-zentiva-50-mg-x-60-compr-elib-prel-5_174334_1_1526890134.jpg.webp)

![[MILURIT 100 mg x 60 COMPR. 100mg EGIS PHARMACEUTICALS][Medicamente cu reteta] MILURIT 100 mg x 60 COMPR. 100mg EGIS PHARMACEUTICALS](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//milurit-100-mg-x-60-compr-100mg-egis-pharmaceutic_174728_1_1531133056.jpg.webp)

![[OLSSA 40 mg/10 mg X 28 COMPR. FILM. 40mg/10mg HCS BVBA - KRKA ][Medicamente cu reteta] OLSSA 40 mg/10 mg X 28 COMPR. FILM. 40mg/10mg HCS BVBA - KRKA](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//olssa-40-mg10-mg-x-28-compr-film-40mg10mg-hcs-_175266_1_1538464166.jpg.webp)

![[TANDESAR 32 mg X 28 COMPR. 32mg TERAPIA S.A.][Medicamente cu reteta] TANDESAR 32 mg X 28 COMPR. 32mg TERAPIA S.A.](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//tandesar-32-mg-x-28-compr-32mg-terapia-sa_175455_1_1540807468.jpg.webp)

![[OVESTIN 0,5 mg X 15 OVULE 0,5 mg ASPEN PHARMA TRADING ][Medicamente cu reteta] OVESTIN 0,5 mg X 15 OVULE 0,5 mg ASPEN PHARMA TRADING](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//ovestin-05-mg-x-15-ovule-05-mg-aspen-pharma-trad_175565_1_1542104959.jpg.webp)

![[DEPAKINE CHRONO 300 mg X 100 COMPR. ELIB. PREL. 300mg SANOFI ROMANIA SRL ][Medicamente cu reteta] DEPAKINE CHRONO 300 mg X 100 COMPR. ELIB. PREL. 300mg SANOFI ROMANIA SRL](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//depakine-chrono-300-mg-x-100-compr-elib-prel-30_176287_1_1551696518.JPG)

![[ZINNAT 500 mg X 10 COMPR. FILM. 500mg GLAXOSMITHKLINE (IRE ][Medicamente cu reteta] ZINNAT 500 mg X 10 COMPR. FILM. 500mg GLAXOSMITHKLINE (IRE](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//zinnat-500-mg-x-10-compr-film-500mg-glaxosmithkl_177311_1_1562066072.jpg.webp)

![[VENTOLIN 100 INHALER CFC-FREE X 1 SUSP. INHAL. PRESURIZATA 100µg/doza GLAXOSMITHKLINE (IRE ][Medicamente cu reteta] VENTOLIN 100 INHALER CFC-FREE X 1 SUSP. INHAL. PRESURIZATA 100µg/doza GLAXOSMITHKLINE (IRE](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//ventolin-100-inhaler-cfcfree-x-1-susp-inhal-pre_177318_1_1562137727.jpg.webp)

![[SERETIDE DISKUS 50 micrograme/100 micrograme X 1 PULB. INHAL. ][Medicamente cu reteta] SERETIDE DISKUS 50 micrograme/100 micrograme X 1 PULB. INHAL.](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//seretide-diskus-50-micrograme100-micrograme-x-1-p_177342_1_1562229928.jpg.webp)

![[THYROZOL 20mg X 50 COMPR. FILM.][Medicamente cu reteta] THYROZOL 20mg X 50 COMPR. FILM.](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//thyrozol-20mg-x-50-compr-film_180617_1_1596109867.jpg.webp)

![[DAVIA 10 mg x 30 COMPR. FIL 10mg TERAPIA][Medicamente cu reteta] DAVIA 10 mg x 30 COMPR. FIL 10mg TERAPIA](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//davia-10-mg-x-30-compr-fil-10mg-terapia_184174_1_1636020614753.jpg.webp)

![[RASAGILINA RATIOPHARM 1 mg X 30 COMPR. 1mg TEVA][Medicamente cu reteta] RASAGILINA RATIOPHARM 1 mg X 30 COMPR. 1mg TEVA](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//rasagilina-ratiopharm-1-mg-x-30-compr-1mg-teva_184181_1_16360363080277.jpg.webp)

![[FORXIGA 10 mg X 90 COMPR. FILM. 10mg ASTRAZENECA][Medicamente cu reteta] FORXIGA 10 mg X 90 COMPR. FILM. 10mg ASTRAZENECA](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//forxiga-10-mg-x-90-compr-film-10mg-astrazeneca_184183_1_16850191131779.jpg.webp)

![[RILUTEK 50 mg X 56 COMPR. FILM. 50mg SANOFI][Medicamente cu reteta] RILUTEK 50 mg X 56 COMPR. FILM. 50mg SANOFI](https://cdn.contentspeed.ro/slir/w210/pfarma.websales.ro/cs-content/cs-photos/products/original//rilutek-50-mg-x-56-compr-film-50mg-sanofi_184216_1_16360992824779.jpg.webp)