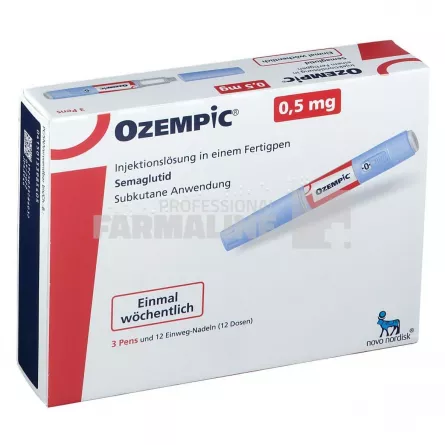
OZEMPIC 0,5 mg X 3
ATENTIE!!!
Acest medicament NU se poate comercializa online.
Se eliberează DOAR DIN FARMACIE, STRICT ÎN BAZA REȚETEI MEDICALE. Se poate rezerva online, cu ridicare din farmacie. Marca: Novo Nordisk A/S
Marca: Novo Nordisk A/S
Descriere
1. DENUMIREA COMERCIALĂ A MEDICAMENTULUI
Ozempic 0,5 mg soluție injectabilă în stilou injector (pen) preumplut.
2. COMPOZIȚIA CALITATIVĂ ȘI CANTITATIVĂ
Ozempic 0,5 mg soluție injectabilă
Un ml soluție conține semaglutidă* 1,34 mg. Un stilou injector (pen) preumplut conține semaglutidă* 2 mg, în 1,5 ml soluție. Fiecare doză conține semaglutidă 0,5 mg în 0,37 ml soluție.
*analog al peptidei umane 1, asemănătoare glucagonului (GLP-1), produs pe celulele de Saccharomyces cerevisiae, prin tehnologia ADN recombinant.
Pentru lista tuturor excipienților, vezi pct. 6.1.
3. FORMA FARMACEUTICĂ
Soluție injectabilă (injecție).
Soluție limpede și incoloră sau aproape incoloră, izotonă; pH=7,4.
4. DATE CLINICE
4.1 Indicații terapeutice
Ozempic este indicat pentru tratamentul adulților cu diabet zaharat de tip 2 insuficient controlat, ca tratament adjuvant la dietă și exerciții fizice:
• sub formă de monoterapie atunci când administrarea de metformin este considerată inadecvată din cauza intoleranței sau contraindicațiilor
• în asociere cu alte medicamente utilizate pentru tratamentul diabetului zaharat.
Pentru informații privind rezultatele studiului în ceea ce privește asocierile terapeutice, efectele asupra controlului glicemic și evenimentele cardiovasculare, precum și grupele de pacienți studiate, vezi pct. 4.4, 4.5 și 5.1.
4.2 Doze și mod de administrare
Doze
Doza inițială este de 0,25 mg semaglutidă, administrată o dată pe săptămână. După 4 săptămâni, doza trebuie crescută la 0,5 mg, administrată o dată pe săptămână. După cel puțin 4 săptămâni de tratament cu o doză de 0,5 mg o dată pe săptămână, doza poate fi crescută la 1 mg, o dată pe săptămână, pentru a realiza un control glicemic mai bun.
Doza de semaglutidă 0,25 mg nu reprezintă o doză de întreținere. Administrarea săptămânală de doze mai mari de 1 mg nu este recomandată.
Când Ozempic este adăugat la tratamentul existent cu metformin și/sau tiazolidindionă, dozele uzuale de metformin și/sau tiazolidindionă pot rămâne neschimbate.
Când se adaugă Ozempic la tratamentul existent cu sulfoniluree sau insulină, trebuie luată în considerare reducerea dozei de sulfoniluree sau insulină, pentru a reduce riscul apariției hipoglicemiei (vezi pct. 4.4 și 4.8).
Nu este necesară auto-monitorizarea glucozei din sânge în vederea ajustării dozei de Ozempic.
Auto-monitorizarea glucozei din sânge este necesară în vederea ajustării dozei de sulfoniluree sau de insulină, mai ales atunci când se începe tratamentul cu Ozempic și se reduce doza de insulină. Se recomandă o strategie etapizată de reducere a dozei de insulină.
Doză omisă
Dacă este omisă o doză, aceasta trebuie administrată cât mai curând posibil și în decurs de 5 zile după omitere. Dacă au trecut mai mult de 5 zile, trebuie să se renunțe la doza omisă, iar următoarea doză trebuie administrată în ziua programată. În fiecare caz, pacienții își pot relua schema terapeutică obișnuită, cu administrare o dată pe săptămână.
Grupe speciale de pacienți
Vârstnici
Nu este necesară ajustarea dozei în funcție de vârstă. Experiența terapeutică privind utilizarea la pacienții cu vârsta ≥75 de ani este limitată (vezi pct. 5.2).
Insuficiență renală
La pacienții cu insuficiență renală ușoară, moderată sau severă nu este necesară ajustarea dozei.
Experiența privind utilizarea semaglutidei la pacienții cu insuficiență renală severă este limitată.
Semaglutida nu este recomandată pentru utilizare la pacienți cu boală renală în stadiu terminal (vezi pct. 5.2).
Insuficiență hepatică
La pacienții cu insuficiență hepatică nu este necesară ajustarea dozei. Experiența privind utilizarea semaglutidei la pacienții cu insuficiență hepatică severă este limitată. Se recomandă prudență la tratarea acestor pacienți cu semaglutidă (vezi pct. 5.2).
Copii și adolescenți
Siguranța și eficacitatea semaglutidei la copii și adolescenți cu vârsta sub 18 ani nu au fost încă stabilite. Nu sunt disponibile date.
Mod de administrare
Ozempic se administrează o dată pe săptămână, la orice oră, cu sau fără alimente.
Ozempic se injectează subcutanat, la nivelul abdomenului, coapselor sau în partea superioară a brațelor. Locul injectării poate fi modificat, fără a fi necesară ajustarea dozei. Ozempic nu trebuie administrat intravenos sau intramuscular.
Ziua administrării săptămânale poate fi modificată dacă este necesar, atât timp cât perioada dintre administrarea a două doze este de cel puțin 3 zile (>72 ore). După selectarea unei noi zile de administrare, trebuie continuată administrarea o dată pe săptămână.
Pentru informații suplimentare privind administrarea, vezi pct. 6.6.
4.3 Contraindicații
Hipersensibilitate la substanța activă sau la oricare dintre excipienții enumerați la pct.6.1.
4.4 Atenționări și precauții speciale pentru utilizare
Semaglutida nu trebuie utilizată la pacienții cu diabet zaharat de tip 1 sau în tratamentul cetoacidozei diabetice. Semaglutida nu este un substitut pentru insulină. Cetoacidoza diabetică a fost raportată la pacienții insulino-dependenți care au avut întreruperea sau reducerea rapidă a dozei de insulină atunci când se începe tratamentul cu un agonist de receptor GLP-1 (vezi pct. 4.2).
Nu există experiență privind utilizarea la pacienții cu insuficiență cardiacă congestivă clasa IV NYHA și, de aceea, semaglutida nu este recomandată la acești pacienți.
Efecte gastrointestinale
Utilizarea agoniștilor de receptor GLP-1 poate fi asociată cu reacții adverse gastrointestinale. Acest fapt trebuie avut în vedere atunci când sunt tratați pacienți cu disfuncție renală, deoarece greața, vărsăturile și diareea pot duce la deshidratare, ce ar putea deteriora funcția renală (vezi pct. 4.8).
Pancreatită acută
Pancreatită acută a fost observată în asociere cu utilizarea agoniștilor de receptor GLP-1. Pacienții trebuie informați asupra simptomatologiei caracteristice pancreatitei acute. Dacă se suspectează pancreatita, administrarea semaglutidei trebuie întreruptă; dacă este confirmată, administrarea semaglutidei nu trebuie reluată. La pacienții cu antecedente de pancreatită se recomandă prudență.
Hipoglicemie
Pacienții tratați cu semaglutidă în asociere cu o sulfoniluree sau insulină pot prezenta un risc crescut de hipoglicemie. Riscul de hipoglicemie poate fi redus prin scăderea dozei de sulfoniluree sau insulină la inițierea tratamentului cu semaglutidă (vezi pct. 4.8).
Retinopatie diabetică
La pacienții cu retinopatie diabetică tratați cu insulină și semaglutidă s-a observat un risc crescut de apariție a complicațiilor retinopatiei diabetice (vezi pct. 4.8). Se recomandă prudență la utilizarea semaglutidei la pacienții cu retinopatie diabetică tratați cu insulină. Acești pacienți trebuie monitorizați cu atenție și tratați în conformitate cu recomandările clinice. Îmbunătățirea rapidă a controlului glicemic a fost asociată cu o agravare temporară a retinopatiei diabetice, dar nu pot fi excluse alte mecanisme.
Conținutul de sodiu
Acest medicament conține sodiu mai puțin de 1 mmol (23 mg) per doză, adică practic „nu conține sodiu”.
4.5 Interacțiuni cu alte medicamente și alte forme de interacțiune
Semaglutida încetinește evacuarea gastrică și poate să influențeze absorbția medicamentelor administrate concomitent, pe cale orală. Semaglutida trebuie utilizată cu prudență la pacienții cărora li se administrează oral medicamente care necesită o absorbție gastrointestinală rapidă.
Paracetamol
Semaglutida reduce viteza de evacuare gastrică, fapt evaluat prin farmacocinetica paracetamolului în timpul unui test alimentar standardizat. ASC0-60min și Cmax ale paracetamolului au scăzut cu 27% și, respectiv, 23%, după administrarea concomitentă de semaglutidă 1 mg. Expunerea totală la paracetamol (ASC0-5ore) nu a fost modificată. Nu este necesară ajustarea dozei de paracetamol, atunci când se administrează concomitent cu semaglutidă.
Contraceptive orale
Nu este de așteptat ca semaglutida să diminueze efectul contraceptivelor orale, deoarece semaglutida nu a modificat expunerea totală la etinilestradiol și levonorgestrel la un nivel relevant din punct de vedere clinic, atunci când s-a administrat concomitent un contraceptiv oral combinat (0,03 mg etinilestradiol/0,15 mg levonorgestrel) cu semaglutida. Expunerea la etinilestradiol nu a fost modificată; la starea de echilibru, a fost observată o creștere de 20% a expunerii la levonorgestrel. Cmax nu a fost influențată, pentru niciuna dintre substanțele active.
Atorvastatină
Semaglutida nu a modificat expunerea totală la atorvastatină după administrarea unei doze unice de atorvastatină (40 mg). Cmax a atorvastatinei a fost scăzută cu 38%. Acest lucru a fost considerat irelevant din punct de vedere clinic.
Digoxină
Semaglutida nu a modificat expunerea totală la digoxină sau Cmax a digoxinei, după administrarea unei doze unice de digoxină (0,5 mg).
Metformin
Semaglutida nu a modificat expunerea totală la metformin sau Cmax a metforminului, după administrarea unei doze de 500 mg, de două ori pe zi, timp de 3,5 zile.
Warfarină
Semaglutida nu a modificat expunerea totală la R- și S-warfarină sau Cmax ale R- și S-warfarinei, după administrarea unei doze unice de warfarină (25 mg), iar efectele farmacodinamice ale warfarinei, măsurate prin raportul internațional normalizat (INR), nu au fost modificate într-o manieră relevantă din punct de vedere clinic. Cu toate acestea, după inițierea terapiei cu semaglutidă, la pacienții tratați cu warfarină sau alți derivați cumarinici se recomandă monitorizarea frecventă a INR.
4.6 Fertilitatea, sarcina și alăptarea
Femei aflate la vârsta fertilă
Se recomandă ca femeile aflate la vârsta fertilă să utilizeze măsuri contraceptive, în cursul tratamentului cu semaglutidă.
Sarcina
Studiile la animale au evidențiat efecte toxice asupra funcției de reproducere (vezi pct. 5.3). Datele provenite din utilizarea semaglutidei la femeile gravide sunt limitate. De aceea, semaglutida nu trebuie utilizată în timpul sarcinii. Dacă o pacientă intenționează să rămână gravidă sau este gravidă, tratamentul cu semaglutidă trebuie întrerupt. Administrarea de semaglutidă trebuie întreruptă cu cel puțin 2 luni înainte de o sarcină planificată, din cauza timpului de înjumătățire plasmatică prelungit (vezi pct. 5.2).
Alăptarea
La femelele șobolan cu lactație, semaglutida a fost excretată în lapte. Deoarece nu se poate exclude un risc pentru un copil hrănit la sân, semaglutida nu trebuie utilizată în timpul alăptării.
Fertilitatea
Nu se cunoaşte efectul semaglutidei asupra fertilității la om. Semaglutida nu a afectat fertilitatea la șobolanii masculi. La femelele șobolan, s-a observat o creștere a perioadei de receptivitate și o ușoară micșorare a numărului de ovulații, în cazul administrării de doze asociate cu pierderea de masă corporală maternă (vezi pct. 5.3).
4.7 Efecte asupra capacității de a conduce vehicule și de a folosi utilaje
Semaglutida nu are nicio influență sau are influență neglijabilă asupra capacității de a conduce vehicule sau de a folosi utilaje. Atunci când se utilizează în asociere cu o sulfoniluree sau insulină, pacienții trebuie informați despre măsurile de precauție necesare pentru a evita hipoglicemia, atunci când conduc vehicule și folosesc utilaje (vezi pct. 4.4).
4.8 Reacții adverse
Rezumatul profilului de siguranță
În 8 studii de fază 3a, 4792 de pacienți au fost expuși la semaglutidă. În timpul studiilor clinice, cele mai frecvente reacții adverse raportate au fost tulburările gastrointestinale, inclusiv greața (foarte frecventă), diareea (foarte frecventă) și vărsăturile (frecvente). În general, severitatea acestor reacții a fost ușoară sau moderată și reacțiile au fost de durată scurtă.
Lista tabelară a reacțiilor adverse
În tabelul 1 sunt prezentate reacțiile adverse identificate în toate studiile de fază 3a, la pacienți cu diabet zaharat de tip 2 (descrise pe larg la pct. 5.1). Frecvențele reacțiilor adverse se bazează pe un grup de studii de fază 3a, cu excepția studiului pentru evaluarea consecințelor cardiovasculare (pentru detalii suplimentare, consultați textul de sub tabel).
Reacțiile sunt enumerate mai jos în funcție de clasificarea pe aparate, sisteme și organe și de frecvența absolută. Categoriile de frecvență sunt definite ca fiind: foarte frecvente (≥1/10); frecvente (≥1/100 și <1/10); mai puțin frecvente (≥1/1000 și <1/100); rare (≥1/10000 și <1/1000) și foarte rare (<1/10000).
În cadrul fiecărei clase de frecvență, reacțiile adverse sunt prezentate în ordinea descrescătoare a gravității.
Studiu clinic cu durata de 2 ani pentru evaluarea consecințelor și siguranței cardiovasculare
La populația cu risc cardiovascular crescut, profilul reacțiilor adverse a fost similar cu cel observat în celelalte studii de fază 3a (descrise la pct. 5.1).
Descrierea reacțiilor adverse selectate
Hipoglicemie
Nu s-au observat episoade hipoglicemice severe în cazurile în care a fost utilizată semaglutida ca monoterapie. Hipoglicemia severă a fost observată mai întâi atunci când semaglutida a fost asociată cu o sulfoniluree (1,2% dintre subiecți, 0,03 evenimente/pacient și an) sau cu insulină (1,5% dintre subiecți, 0,02 evenimente/pacient și an). Puține episoade (0,1% dintre subiecți, 0,001 evenimente/pacient și an) au fost observate în cazul administrării semaglutidei în asociere cu antidiabetice orale, altele decât sulfoniluree.
Reacții adverse gastrointestinale
Greața a apărut la 17,0% dintre pacienții tratați cu semaglutidă 0,5 mg și la 19,9% dintre pacienții tratați cu semaglutidă 1 mg, diareea la 12,2% și, respectiv, 13,3% iar vărsăturile la 6,4% și, respectiv, 8,4%. Majoritatea acestor evenimente au avut severitate ușoară sau moderată și au fost de durată scurtă. Evenimentele au dus la întreruperea tratamentului la 3,9% și, respectiv, 5% dintre pacienți.
Evenimentele au fost raportate cel mai frecvent în primele luni de tratament.
Pacienții cu greutate corporală redusă pot prezenta mai multe reacții adverse gastrointestinale atunci când sunt tratați cu semaglutidă.
Pancreatită acută
Frecvenţa pancreatitei acute confirmate prin adjudecare, raportată în studiile clinice de fază 3a, a fost de 0,3% pentru semaglutidă şi, respectiv, de 0,2% pentru comparator. În studiul rezultatelor cardiovasculare (CVOT) la 2 ani, frecvența pancreatitei acute confirmate prin adjudecare a fost de 0,5% pentru semaglutidă și de 0,6% pentru placebo (vezi pct. 4.4).
Complicații ale retinopatiei diabetice
Un studiu clinic cu durata de 2 ani a investigat 3297 de pacienți cu diabet zaharat de tip 2, cu risc cardiovascular crescut, cu un istoric îndelungat de diabet și cu valori ale glicemiei slab controlate. În acest studiu, au apărut evenimente considerate a fi complicații ale retinopatiei diabetice la mai mulți pacienți tratați cu semaglutidă (3,0%), comparativ cu placebo (1,8%). Acest lucru a fost observat la pacienții cu retinopatie diabetică cunoscută, tratați cu insulină. Diferența de tratament a apărut devreme și a persistat pe tot parcursul studiului. Evaluarea sistematică a complicațiilor retinopatiei diabetice a fost efectuată doar în studiul cardiovascular. În studiile clinice cu durata de până la 1 an, care au inclus 4807 pacienți cu diabet zaharat de tip 2, evenimentele adverse legate de retinopatia diabetică au fost raportate în procente similare la subiecții tratați cu semaglutidă (1,7%) și la subiecții din grupul comparator (2,0%).
Întreruperea tratamentului din cauza unui eveniment advers
Incidența întreruperii tratamentului din cauza evenimentelor adverse a fost de 6,1% la pacienții tratați cu semaglutidă 0,5 mg și de 8,7% la pacienții tratați cu semaglutidă 1 mg, față de 1,5% în cazul administrării de placebo. Cele mai frecvente evenimente adverse care au dus la întreruperea tratamentului au fost gastrointestinale.
Reacții adverse la nivelul locului de injectare
Reacțiile la nivelul locului de injectare (de exemplu erupție cutanată la nivelul locului de injectare, eritem) au fost raportate de 0,6% dintre pacienții cărora li s-a administrat semaglutidă 0,5 mg și de 0,5% dintre pacienții cărora li s-a administrat semaglutidă 1 mg. Aceste reacții au fost de obicei ușoare.
Imunogenitate
În concordanță cu proprietățile potențial imunogene ale medicamentelor care conțin proteine sau peptide, pacienții pot dezvolta anticorpi ca urmare a tratamentului cu semaglutidă. Procentul de pacienți testați pozitiv pentru anticorpi anti-semaglutidă, în orice moment după momentul inițial, a fost redus (1-2%) și, la sfârșitul studiului, niciun pacient nu a prezentat anticorpi neutralizanți antisemaglutidă sau anticorpi anti-semaglutidă cu efect neutralizant endogen GLP-1.
Creșterea frecvenței cardiace
Creșterea frecvenței cardiace a fost observată la agoniști ai receptorilor GLP-1. În studiile clinice de fază 3a, au fost observate la subiecți tratați cu Ozempic creșteri medii de 1 până la 6 bătăi pe minut (bpm) de la o valoare de bază de 72 până la 76 bpm. Într-un studiu de lungă durată la subiecți cu factori de risc cardiovascular, 16% dintre subiecții tratați cu Ozempic au avut o creștere a frecvenței cardiace de >10 bpm, comparativ cu 11% dintre subiecții cărora li s-a administrat placebo, după 2 ani de tratament.
Raportarea reacțiilor adverse suspectate
Este importantă raportarea reacțiilor adverse suspectate după autorizarea medicamentului. Acest lucru permite monitorizarea continuă a raportului beneficiu/risc al medicamentului. Profesioniștii din domeniul sănătății sunt rugați să raporteze orice reacție adversă suspectată prin intermediul sistemului național de raportare, astfel cum este menționat în Anexa V.
4.9 Supradozaj
În studiile clinice au fost raportate supradozaje cu utilizarea unei doze de până la 4 mg într-o singură priză și de până la 4 mg pe săptămână. Cea mai frecventă reacție adversă raportată a fost greața. Toți pacienții s-au recuperat fără complicații.
Nu există un antidot specific pentru supradozajul cu semaglutidă. În caz de supradozaj, trebuie inițiat tratamentul de susținere corespunzător, în funcție de semnele și simptomele clinice ale pacientului.
Poate fi necesară o perioadă prelungită de monitorizare și tratament pentru aceste simptome, luând în considerare timpul de înjumătățire plasmatică prelungit al semaglutidei, de aproximativ 1 săptămână (vezi pct. 5.2).
5. PROPRIETĂȚI FARMACOLOGICE
5.1 Proprietăți farmacodinamice
Grupa farmacoterapeutică: medicamente utilizate în diabetul zaharat, analogi ai peptidei 1 asemănătoare glucagonului (GLP-1), codul ATC: A10BJ06
Mecanism de acțiune
Semaglutida este un analog GLP-1, cu structură identică în proporție de 94% cu GLP-1 uman.
Semaglutida acționează ca agonist al receptorului GLP-1 ce se leagă selectiv și activează receptorul GLP-1, ținta pentru GLP-1 endogen. GLP-1 este un hormon fiziologic, cu multiple acțiuni în reglarea glicemiei și apetitului, și cu efecte asupra sistemului cardiovascular. Acțiuni ce țin de reglarea glicemiei și apetitului sunt mediate în mod specific prin receptorii GLP-1 de la nivelul pancreasului și creierului.
Semaglutida reduce glicemia, într-un mod dependent de concentrația plasmatică glucoză, prin stimularea secreției de insulină și prin reducerea secreției de glucagon, atunci când glicemia are valori mari. Mecanismul de scădere a concentrației de glucoză din sânge implică, de asemena, o ușoară încetinire a evacuării gastrice în faza postprandială precoce. În caz de hipoglicemie, semaglutida reduce secreția de insulină și nu inhibă secreția de glucagon.
Semaglutida reduce greutatea corporală și masa de țesut adipos printr-un aport energetic mai redus, implicând un apetit general redus. În plus, semaglutida scade preferința pentru alimentele bogate în grăsimi.
Receptorii GLP-1 sunt, de asemenea, exprimați la nivelul cordului, sistemului vascular, sistemului imunitar și rinichilor.
În studiile clinice, semaglutida a avut un efect benefic asupra concentrațiilor plasmatice ale lipidelor, a scăzut tensiunea arterială sistolică și a limitat inflamația. În studiile efectuate la animale, semaglutida a redus dezvoltarea aterosclerozei prin împiedicarea progresiei plăcii la nivelul aortei și prin reducerea inflamației la nivelul plăcii.
Efecte farmacodinamice
Toate evaluările farmacodinamice au fost efectuate după 12 săptămâni de tratament (inclusiv perioada de creștere a dozei), la starea de echilibru, în cazul administrării de semaglutidă 1 mg o dată pe săptămână.
Glicemie în condiții de repaus alimentar și postprandial
Semaglutida reduce valorile glicemiei în condiții de repaus alimentar și postprandial. La pacienții cu diabet zaharat de tip 2, tratamentul cu semaglutidă 1 mg a determinat o scădere a glicemiei, dacă se face referire la modificarea absolută față de valoarea inițială (mmol/l) și o reducere relativă în comparație cu placebo (%) a glicemiei în condiții de repaus alimentar (1,6 mmol/l; reducere de 22%), a glicemiei la 2 ore postprandial (4,1 mmol/l, reducere de 37%), a concentrației sanguine medii de glucoză pe 24 ore (1,7 mmol/l, reducere de 22%) și la variația glicemiei postprandiale în interval de 3 mese (0,6-1,1 mmol/l), în comparație cu placebo. Semaglutida a scăzut valoarea glicemiei în condiții de repaus alimentar după administrarea primei doze.
Funcția celulelor beta și secreția de insulină
Semaglutida îmbunătățește funcția celulelor beta. În comparație cu placebo, semaglutida a îmbunătățit răspunsul la insulină în prima și a doua fază, cu o creștere de 3 ori și, respectiv, de 2 ori, și a crescut capacitatea secretorie maximă a celulelor beta la pacienții cu diabet zaharat de tip 2. În plus, tratamentul cu semaglutidă a crescut concentrațiile plasmatice de insulină în condiții de repaus alimentar, comparativ cu placebo.
Secreție de glucagon
Semaglutida reduce concentrațiile plasmatice de glucagon în condiții de repaus alimentar și postprandial. La pacienții cu diabet zaharat de tip 2, semaglutida a determinat următoarele reduceri relative ale glucagonului, în comparație cu placebo: glucagon în condiții de repaus alimentar (8-21%), răspunsul postprandial la glucagon (14-15%) și concentrația plasmatică medie pe 24 de ore a glucagonului (12%).
Insulină dependentă de glucoză și secreție de glucagon
Semaglutida a scăzut concentrațiile mari ale glucozei din sânge prin stimularea secreției de insulină și reducerea secreției de glucagon, într-un mod dependent de glucoză. În cazul semaglutidei, rata de secreție a insulinei la pacienții cu diabet zaharat de tip 2 a fost comparabilă cu cea a subiecților sănătoși.
În timpul hipoglicemiei induse, în comparație cu placebo, semaglutida nu a modificat răspunsurile de contrareglare ale secreției crescute de glucagon și nu a influențat scăderea concentrației plasmatice a peptidului C la pacienții cu diabet zaharat de tip 2.
Evacuare gastrică
Semaglutida a provocat o întârziere minoră a evacuării gastrice postprandial precoce, reducând astfel rata la care glucoza apare în circulație postprandial.
Apetitul, consumul de energie și alegerea alimentelor
În comparație cu placebo, semaglutida a scăzut aportul de energie a 3 mese ad libitum consecutive cu 18-35%. Această scădere a fost susținută de o suprimare a apetitului indusă de semaglutidă, în condiții de repaus alimentar, precum și postprandial, un control îmbunătățit al mâncatului, o poftă mai mică pentru alimente și o preferință relativ scăzută pentru alimentele bogate în grăsimi.
Lipidemie în condiții de repaus alimentar și postprandial
Semaglutida, comparativ cu placebo, a redus, în condiții de repaus alimentar, concentrațiile plasmatice ale trigliceridelor și fracției colesterol lipoproteină cu densitate foarte mică (VLDL) cu 12% și, respectiv, 21%. Răspunsul postprandial al concentrațiilor plasmatice ale trigliceridelor și fracției colesterol VLDL, după un prânz bogat în grăsimi, a fost redus cu >40%.
Electrofiziologie cardiacă (QTc)
Efectul semaglutidei asupra repolarizării cardiace a fost testat într-un studiu QTc aprofundat.
Semaglutida nu a prelungit intervalele QTc la doze mai mari decât cele terapeutice (doze de până la 1,5 mg, la starea de echilibru).
Eficacitate și siguranță clinică
Atât îmbunătățirea controlului glicemic, cât și reducerea morbidității și mortalității cardiovasculare, sunt elemente esențiale ale tratamentului diabetului de tip 2.
Eficacitatea și siguranța administrării Ozempic 0,5 mg și 1 mg o dată pe săptămână au fost evaluate în șase studii randomizate controlate de fază 3a, care au inclus 7215 pacienți cu diabet zaharat de tip 2 (4107 pacienți tratați cu semaglutidă). Cinci studii (SUSTAIN 1-5) au avut ca criteriu principal evaluarea eficacității asupra controlului glicemic, în timp ce un studiu (SUSTAIN 6) a avut ca criteriu principal evaluarea rezultatelor cardiovasculare.
Un studiu clinic suplimentar ce a inclus 1201 pacienți a fost efectuat pentru a compara eficacitatea și siguranța Ozempic 0,5 mg și 1 mg o dată pe săptămână cu dulaglutid 0,75 mg și, respectiv, 1,5 mg, o dată pe săptămână.
Tratamentul cu semaglutidă a demonstrat reduceri susținute, superioare statistic și semnificative clinic ale valorilor HbA1c și greutății corporale, timp de până la 2 ani, în comparație cu placebo și cu tratamentul de control cu substanțe active (sitagliptină, insulină glargin, exenatidă ER și dulaglutid).
Eficacitatea semaglutidei nu a fost influențată de vârstă, sex, rasă, etnie, IMC la momentul inițial, masa corporală (kg) la momentul inițial, durata de la diagnosticarea diabetului zaharat și gradul insuficienței renale.
SUSTAIN 1 – Monoterapie
Într-un studiu dublu-orb, controlat cu placebo, cu durata de 30 de săptămâni, 388 pacienți controlați necorespunzător prin dietă și exerciții fizice au fost randomizați pentru administrarea de Ozempic 0,5 mg sau Ozempic 1 mg o dată pe săptămână sau placebo.
Boli cardiovasculare
Într-un studiu clinic dublu-orb, cu durata de 104 săptămâni (SUSTAIN 6), 3297 de pacienți cu diabet zaharat de tip 2 cu risc cardiovascular crescut au fost randomizați pentru administrarea de Ozempic 0,5 mg o dată pe săptămână, Ozempic 1 mg o dată pe săptămână, sau placebo, pe lângă un regim igieno-dietetic standard urmat timp de 2 ani. În total, 98% dintre pacienți au ajuns la finalul studiului, iar starea vitală a fost cunoscută la sfârșitul studiului pentru 99,6% dintre pacienți.
Populația de studiu a fost distribuită pe vârste astfel: 1598 pacienți (48,5%) ≥65 ani, 321 (9,7%) ≥75 ani și 20 (0,6%) ≥85 ani. Dintre aceștia, 2358 de pacienți aveau funcție renală normală sau insuficiență renală ușoară, 832 aveau insuficiență renală moderată și 107 aveau insuficiență renală severă sau boală renală în stadiu terminal. 61% dintre pacienți erau bărbați, vârsta medie a fost de 65 de ani și valoarea medie a IMC a fost de 33 kg/m2 . Durata medie de la diagnosticarea diabetului zaharat era de 13,9 ani.
Criteriul principal de evaluare a fost timpul de la randomizare până la apariția primului eveniment advers cardiovascular major (EACM): decesul de cauză cardiovasculară, infarctul miocardic non-letal sau accidentul vascular cerebral non-letal.
Greutate corporală
După un an de tratament, a fost obținută o scădere în greutate de ≥5% și ≥10% la mai mulți subiecți tratați cu Ozempic 0,5 mg (46% și 13%) și 1 mg (52-62% și 21-24%) comparativ cu pacienții tratați cu comparatorii activi sitagliptină (18% și 3%) și exenatidă EP (17% și 4%).
În studiul clinic cu durata de 40 săptămâni comparativ cu dulaglutid, a fost obținută o scădere în greutate de ≥5% și ≥10% pentru mai mulți pacienți cu Ozempic 0,5 mg (44% și 14%) comparativ cu dulaglutid 0,75 mg (23% și 3%) și Ozempic 1 mg ( până la 63% și 27%) comparativ cu dulaglutid 1,5 mg (30% și 8%).
În studiul SUSTAIN 6 a fost observată o reducere semnificativă și susținută a greutății corporale de la momentul inițial și până în săptămâna 104 în grupurile de tratament cu Ozempic 0,5 mg și 1 mg, față de administrarea de placebo 0,5 mg și 1 mg, acestea fiind administrate în plus față de standardul de îngrijire (-3,6 kg și -4,9 kg față de -0,7 kg și, respectiv, -0,5 kg).
Tensiune arterială
S-au observat reduceri semnificative ale tensiunii arteriale sistolice medii când au fost utilizate Ozempic 0,5 mg (3,5-5,1 mmHg) și 1 mg (5,4-7,3 mmHg) în asociere cu medicamente antidiabetice orale sau insulină bazală. Pentru tensiunea arterială diastolică, nu au existat diferențe semnificative între semaglutidă și comparatori.
Copii și adolescenți
Agenția Europeană pentru Medicamente a suspendat temporar obligația de depunere a rezultatelor studiilor efectuate cu semaglutidă la una sau mai multe subgrupe de copii și adolescenți cu diabet zaharat tip 2 (vezi pct. 4.2).
5.2 Proprietăți farmacocinetice
În comparație cu GLP-1 endogen, semaglutida are un timp de înjumătățire plasmatică prelungit, de aproximativ 1 săptămână, ceea ce o face potrivită pentru administrarea subcutanată o dată pe săptămână. Mecanismul principal al prelungirii acțiunii este legarea de albumina plasmatică, care determină scăderea clearance-ului renal și protecția împotriva degradării metabolice. Mai mult, semaglutida este stabilizată împotriva degradării prin enzima DPP-4.
Absorbție
Concentrația plasmatică maximă a fost atinsă la 1 până la 3 zile după administrarea dozei. Expunerea la starea de echilibru a fost realizată după 4-5 săptămâni de administrare o dată pe săptămână. La pacienții cu diabet zaharat de tip 2, concentrațiile plasmatice medii, la starea de echilibru, după administrarea subcutanată a dozelor de semaglutidă de 0,5 mg și 1 mg au fost de aproximativ 16 nmol/l și, respectiv, 30 nmol/l. Expunerea la semaglutidă a crescut în mod proporțional cu doza, în cazul administrării de doze de 0,5 mg și 1 mg. Prin administrarea subcutanată a semaglutidei la nivelul abdomenului, coapselor sau părții superioară a brațului au fost obținute expuneri similare.
Biodisponibilitatea absolută a semaglutidei în cazul administrării subcutanate a fost de 89%.
Distribuție
Volumul mediu de distribuție al semaglutidei, după administrarea subcutanată la pacienții cu diabet zaharat de tip 2, a fost de aproximativ 12,5 l. Semaglutida se leagă în proporție foarte mare de proteinele plasmatice (>99%).
Metabolizare
Înainte de excreție, semaglutida este metabolizată în proporție foarte mare prin clivarea proteolitică a catenei peptidice și beta-oxidarea secvențială a lanțului lateral al acidului gras. Se estimează că endopeptidaza neutră (NEP) este implicată în metabolizarea semaglutidei.
Eliminare
Într-un studiu cu administrare subcutanată a unei doze unice de semaglutidă marcată radioactiv, s-a constatat că principalele căi de excreție ale compusului semaglutidic au fost prin urină și materii fecale; aproximativ 2/3 din compusul semaglutidic au fost excretate în urină și aproximativ 1/3 în materiile fecale. Aproximativ 3% din doză a fost excretată sub formă de semaglutidă nemetabolizată prin urină. La pacienții cu diabet zaharat de tip 2, clearance-ul semaglutidei a fost de aproximativ 0,05 l/oră. Având un timp de înjumătățire plasmatică prin eliminare de aproximativ 1 săptămână, semaglutida va fi prezentă în circulația sanguină timp de aproximativ 5 săptămâni după administrarea ultimei doze.
Grupe speciale de pacienți
Vârstnici
Vârsta nu a avut niciun efect asupra farmacocineticii semaglutidei, pe baza datelor din studiile de fază 3a ce au inclus pacienți cu vârsta cuprinsă între 20 și 86 de ani.
Sex, rasă și etnie
Sexul, rasa (albă, de culoare sau afro-americani, asiatică) și etnia (hispanic sau latino, non-hispanic sau –latino) nu au avut niciun efect asupra farmacocineticii semaglutidei.
Greutate corporală
Greutatea corporală are efect asupra expunerii la semaglutidă. Greutatea corporală mai mare duce la o expunere mai scăzută; o diferență de 20% în ceea ce privește greutatea corporală între indivizi va determina o diferență de aproximativ 16% a expunerii. Dozele de 0,5 mg și 1 mg de semaglutidă asigură o expunere sistemică adecvată pentru greutăți corporale cuprinse între 40-198 kg.
Insuficiență renală
Insuficiența renală nu a influențat farmacocinetica semaglutidei într-o manieră clinică relevantă. Acest lucru a fost demonstrat în cazul administrării unei doze unice de semaglutidă 0,5 mg la pacienți cu grade diferite de insuficiență renală (ușoară, moderată, severă sau pacienți care efectuează ședințe de dializă), comparativ cu subiecții cu funcție renală normală. De asemenea, acest lucru a fost demonstrat la subiecții cu diabet zaharat de tip 2 și cu insuficiență renală, pe baza datelor din studiile de fază 3a, deși experiența la pacienții cu boală renală în stadiu terminal a fost limitată.
Insuficiență hepatică
Insuficiența hepatică nu a avut niciun impact asupra expunerii la semaglutidă. Farmacocinetica semaglutidei a fost evaluată la pacienți cu grade diferite de insuficiență hepatică (ușoară, moderată, severă), comparativ cu subiecții cu funcție hepatică normală, într-un studiu în care s-a administrat o doză unică de semaglutidă 0,5 mg.
Copii și adolescenți
Semaglutida nu a fost studiată la copii și adolescenți.
5.3 Date preclinice de siguranță
Datele preclinice nu au evidențiat riscuri speciale pentru om pe baza studiilor convenționale farmacologice privind evaluarea siguranței, toxicitatea după doze repetate sau genotoxicitatea. Tumorile non-letale ale celulelor C ale tiroidei observate la rozătoare sunt un efect de clasă pentru agoniștii receptorului GLP-1. În studiile pentru determinarea caracterului cancerigen, efectuate pe o durată de 2 ani, la șobolani și șoareci, semaglutida a provocat tumori non-letale ale celulelor C ale tiroidei. Nu au fost observate alte tumori apărute în urma tratamentului. Tumorile cu celule C la rozătoare sunt determinate printr-un mecanism non-genotoxic, mediat de un receptor specific GLP-1, la care rozătoarele sunt sensibile în mod deosebit. Relevanța pentru om este considerată a fi mică, dar nu poate fi exclusă complet.
În studiile de fertilitate efectuate la șobolani, semaglutida nu a afectat performanța de împerechere sau fertilitatea la șobolanii masculi. La femelele șobolan, s-a observat o creștere a perioadei de receptivitate și o ușoară reducere a numărului de corpi luteali (ovulații), la doze asociate cu pierderea în greutate corporală maternă.
În studiile de dezvoltare embrio-fetală efectuate la șobolani, semaglutida a determinat o embriotoxicitate la valori sub expunerile relevante din punct de vedere clinic. Semaglutida a determinat reduceri semnificative ale greutății corporale materne și reducerea supraviețuirii și creșterii embrionare. La fetus s-au observat malformații scheletale și viscerale majore, incluzând efecte asupra oaselor lungi, coastelor, vertebrelor, cozii, vaselor de sânge și ventriculilor cerebrali. La șobolan, evaluările mecanismelor au indicat că embriotoxicitatea a implicat o afectare mediată de receptorul GLP-1 a alimentării cu nutrienți a embrionului în sacul vitelin. Datorită diferențelor anatomice și funcționale ale sacului vitelin între specii și datorită lipsei expresiei receptorului GLP-1 în sacul vitelin la primatele non-umanoide, se consideră că este puțin probabil ca acest mecanism să fie relevant pentru om. Cu toate acestea, nu poate fi exclus un efect direct al semaglutidei asupra fătului.
În studiile de toxicitate asupra dezvoltării efectuate la iepuri și maimuțe Cynomolgus, a fost observată o creștere a incidenței avorturilor și o incidență ușor crescută a anomaliilor fetale, la expuneri relevante clinic. Constatările au coincis cu o pierdere marcată a greutății corporale, de până la 16%.
Nu se cunoaște dacă aceste efecte sunt legate de scăderea consumului alimentar matern, ca efect direct al GLP-1.
Creșterea și dezvoltarea postnatală au fost evaluate la maimuțele Cynomolgus. Puii au fost puțin mai mici la naștere, dar au recuperat în timpul perioadei de alăptare.
La puii de șobolani, semaglutida a determinat maturizare sexuală întârziată atât la masculi, cât și la femele. Aceste întârzieri nu au avut niciun impact asupra fertilității și capacității de reproducere, indiferent de sex sau asupra capacității femelelor de a menține sarcina.
6. PROPRIETĂȚI FARMACEUTICE
6.1 Lista excipienților
Fosfat disodic dihidrat
Propilen glicol
Fenol
Acid clorhidric (pentru ajustarea pH-ului)
Hidroxid de sodiu (pentru ajustarea pH-ului)
Apă pentru preparate injectabile
6.2 Incompatibilități
În absența studiilor de compatibilitate, acest medicament nu trebuie amestecat cu alte medicamente.
6.3 Perioada de valabilitate
3 ani.
Perioada de valabilitate în cursul utilizării: 6 săptămâni.
După prima utilizare: A se păstra la temperaturi sub 30°C sau la frigider (între 2°C și 8°C). A nu se congela Ozempic și a nu se utiliza Ozempic dacă a fost congelat. Atunci când nu este utilizat, a se păstra stiloul injector (pen-ul) acoperit cu capac, pentru a fi protejat de lumină.
După fiecare injectare, întotdeauna acul pentru injecție trebuie aruncat și stiloul injector trebuie păstrat fără ac atașat. Acest lucru poate preveni blocarea acelor, contaminarea, infectarea, scurgerea de soluție și administrarea de doze incorecte.
6.4 Precauții speciale pentru păstrare
Înainte de prima utilizare: A se păstra la frigider (între 2°C și 8°C). A se păstra la distanță de elementul de răcire.
A nu se congela Ozempic și a nu se utiliza Ozempic dacă a fost congelat.
Pentru condițiile de păstrare ale medicamentului după prima deschidere, vezi pct. 6.3.
A se păstra stiloul injector (pen-ul) acoperit cu capacul, pentru a fi protejat de lumină.
6.5 Natura și conținutul ambalajului
Cartuș din sticlă cu capacitatea de 1,5 ml sau 3 ml(sticlă de tip I), închis la un capăt cu un piston din cauciuc (clorobutil) și la celălalt capăt cu un capac din aluminiu și folie laminată din cauciuc (bromobutil/poliizopren). Cartușul este montat în stilou injector (pen) preumplut, de unică folosință, confecționat din polipropilenă, polioximetilen, policarbonat și acrilonitril-butadien-stiren.
Mărimimile ambalajului:
Ozempic 0,5 mg soluție injectabilă: fiecare stilou injector (pen) preumplut conține 1,5 ml de soluție, livrând 4 doze de 0,5 mg.
1 stilou injector (pen) preumplut și 4 ace de unică folosință NovoFine Plus
3 stilouri injectoare (pen) preumplute și 12 ace de unică folosință NovoFine Plus
6.6 Precauții speciale pentru eliminarea reziduurilor și alte instrucțiuni de manipulare
Pacientul trebuie sfătuit să arunce acul pentru injecție în conformitate cu cerințele locale, după fiecare injectare și să păstreze stiloul injector (pen-ul) fără acul pentru injecție atașat. Acest lucru poate preveni blocarea acelor, contaminarea, infectarea, scurgerea de soluție și administrarea de doze incorecte. Acele și alte materiale reziduale trebuie eliminate în conformitate cu reglementărilor locale.
Stiloul injector (pen) este conceput pentru a fi utilizat de către o singură persoană.
Ozempic nu trebuie utilizat dacă soluția nu este limpede și incoloră sau aproape incoloră.
Ozempic nu trebuie utilizat dacă a fost congelat.
Ozempic poate fi administrat folosind ace cu o lungime de cel mult 8 mm. Stiloul injector (pen-ul) este conceput pentru a fi utilizat cu ace de unică folosință NovoFine sau NovoTwist. Acele NovoFine Plus sunt incluse în pachet.
7. DEȚINĂTORUL AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
Novo Nordisk A/S
Novo Allé
DK-2880 Bagsværd
Danemarca
8. NUMĂRUL(ELE) AUTORIZAȚIEI DE PUNERE PE PIAȚĂ
EU/1/17/1251/002
EU/1/17/1251/003
EU/1/17/1251/004
EU/1/17/1251/005
EU/1/17/1251/006
9. DATA PRIMEI AUTORIZĂRI SAU A REÎNNOIRII AUTORIZAȚIEI
Data primei autorizări: 08 Februarie 2018
10. DATA REVIZUIRII TEXTULUI
Informații detaliate privind acest medicament sunt disponibile pe site-ul Agenției Europene pentru
Medicamente http://www.ema.europa.eu/.
Review-uri
Pareri OZEMPIC 0,5 mg X 3
Fii primul care sparge gheata!
Spune-ne parerea ta despre acest produs si porneste discutia.
Detii sau ai utilizat produsul?
Clientii pfarma.ro nu au adaugat inca opinii pentru acest produs. Fii primul care adauga o parere, folosind formularul de mai jos.

.jpg.webp)